Vecteurs viraux et transfert de gènes (VVTG)
Transfert de gènes par vecteurs viraux, production à façon de lentivirus, rétrovirus ou adénovirus recombinants, et immortalisation de cellules lymphoïdes B et T.

Vecteurs viraux et transfert de gènes (VVTG)
Transfert de gènes par vecteurs viraux, production à façon de lentivirus, rétrovirus ou adénovirus recombinants, et immortalisation de cellules lymphoïdes B et T.
Vecteurs viraux et transfert de gènes (VVTG)
La plateforme VVTG réalise avec expertise depuis 2009 des prestations de production virale à façon pour les laboratoires de recherche académiques français. Elle offre un service de production et de dosage de virus recombinants de transfert de gènes.
Les virus sont des lentivirus, rétrovirus, adénovirus et virus adénoassociés (AAVr) de grade recherche, défectifs pour la réplication. Ces virus ont la capacité de transférer du matériel génétique dans les cellules cibles infectées pour moduler l’expression de gènes (thérapie additive ou soustractive) ou en modifier la séquence. Les types viraux fournis couvrent de nombreuses applications de transfert de gènes, in vitro et in vivo, avec des conditionnements de production adaptés, des contrôles qualité, des productions virales test et la proposition de divers outils viraux.
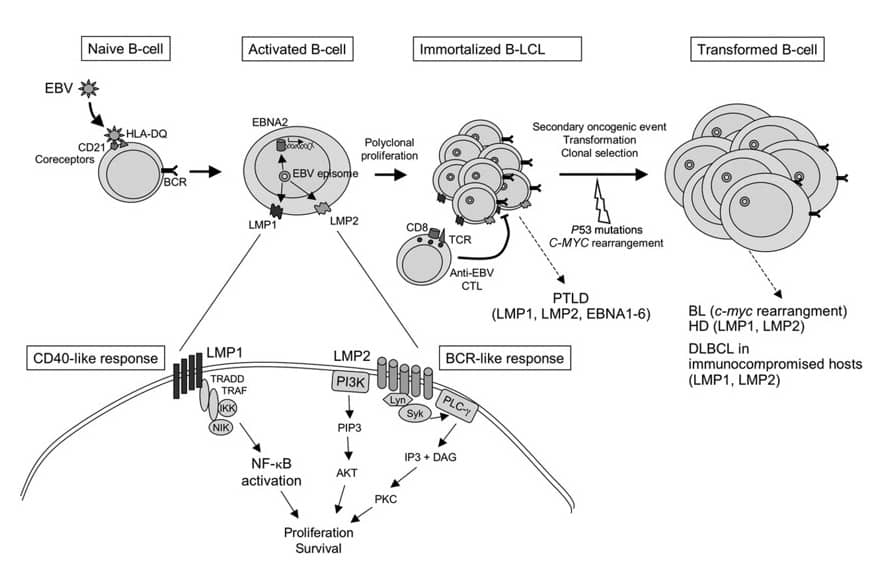
La plateforme propose également un service d’immortalisation de lymphocytes B et T humains à l’aide des virus EBV et Saïmiri en immortalisation simple ou double. Cette prestation, qui peut être réalisée à partir d’un même échantillon de sang, est adaptée aux recherches menées sur les maladies rares qui affectent le système immunitaire.
En plus de ses expertises et services, VVTG met à disposition de ses utilisateurs son laboratoire L3 pour la manipulation de microorganismes, d’OGM et de vecteurs viraux de classe 3.
Expertises et services
Production de vecteurs viraux de transfert de gènes :
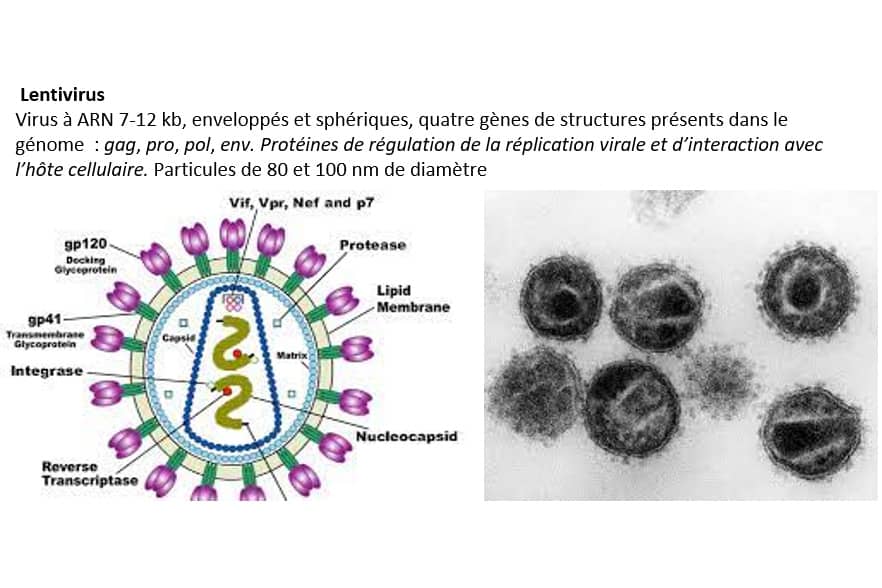
- Production de lentivirus ΔU3 SIN de troisième génération avec enveloppe VSV‐G,
- Production de rétrovirus MLV avec enveloppe VSV‐G ou écotrope,
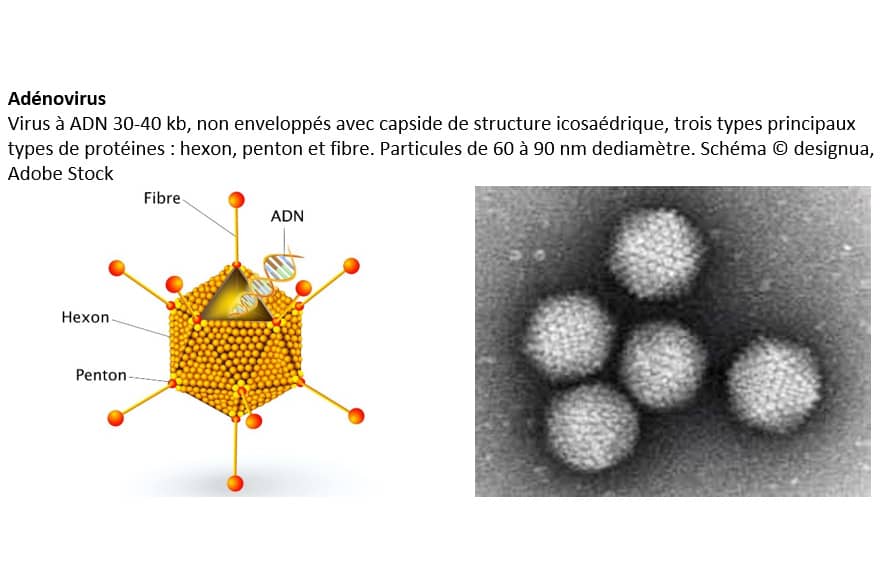
- Production d’adénovirus de sérotype 5, ΔE1 et ΔE3 : application de particules adénovirales existantes, ou obtention de nouvelles constructions (kit AdEasy) puis amplification,
- Production de virus adénoassociés AAV2-8, AAV2-9 et d'autres sérotypes,
- Livraison des virus en conditionnements adaptés aux applications,
- Titres viraux indicatifs : 40 à 250 µL de virus à 10E8 à 10E9 TU ou GI/mL pour les lentivirus, 40 à 250 µL de virus à 10E7 à 10E8 TU/mL pour les rétrovirus, 1 à 5 mL de virus à 10E11 à 10E12 particules virales/mL pour les adénovirus, 20 aliquots de 20 µl de virus purifié à 1014 particules virales/mL pour les AAV2-8 et AAV2-9,
- Conseil sur les vecteurs viraux de transfert de gènes : adaptation des types viraux, sélection des conditionnements, suivi des infections et manipulation des virus en L2 et L3,
- Conseil sur la règlementation des OGM : obtention des agréments d’installation et d’autorisation, transport des OGM et classement des inserts ADN de vecteurs viraux en catégorie A ou B selon leur dangerosité.
Titration et dosage de virus :
- Titration de lentivirus fluorophore par FACS, sélection par antibiotiques et qPCR,
- Titration de rétrovirus fluorophore par FACS et sélection par antibiotiques,
- Titration d’adénovirus par plage de lyse,
- Titration d’AAV2-8 par qPCR et infections in vitro,
- Livraison en carboglace d’aliquots de 10, 20, ou 100 µL de virus congelés à -80°C.
Immortalisation de cellules lymphoïdes :
- Immortalisation de cellules lymphoïdes à partir d’échantillons de sang humain : lymphocytes B (virus EBV) et lymphocytes T (virus Saïmiri),
- Livraison de cellules en culture et d’ampoules de cellules congelées,
- Conseil sur les virus d’immortalisation, la culture des cellules et la règlementation.
Moyens et équipements
- Laboratoire L1 pour les activités de bactériologie et la préparation d’ADN : PSM II, incubateur bactériologique, centrifugeuses, réfrigérateurs et congélateurs,
- Laboratoire L1 pour la biologie moléculaire, la quantification qPCR et la construction de vecteurs : PSM II, incubateur bactériologique, centrifugeuses, réfrigérateurs et congélateurs,
- Laboratoire L2 pour la production d’OGM viraux de groupe 2 classe 2 avec inserts de type A, la culture de cellules humaines, la production de vecteurs viraux et l’immortalisation de cellules lymphocytaires : PSM II, incubateurs à CO2, centrifugeuses, ultracentrifugeuses, réfrigérateurs, congélateurs à -20°C et -80°C, microscopes et sonificateur,
- Laboratoire L3 pour la manipulation de microorganismes ou d’OGM de classe 3 et la production de vecteurs viraux de classe 3 : PSM II, incubateurs à CO2, incubateurs bactériologiques, centrifugeuses et ultracentrifugeuses, réfrigérateurs, congélateurs à -20°C et -80°C, microscope avec caméra et ordinateur.
Comment soumettre un projet ?
Pour soumettre une demande de prestation, vous pouvez prendre contact avec Sylvie Fabrega, responsable technique de la plateforme VVTG. Vous recevrez des documents d’information sur les prestations proposées et les modalités des projets collaboratifs, ainsi qu’un formulaire de demande de prestation à remplir. Un devis et un calendrier prévisionnel seront ensuite établis pour cadrer les manipulations à réaliser. Les résultats obtenus vous seront transmis en fin de prestation. Vous serez alors sollicités pour le règlement de la prestation et le suivi de la valorisation scientifique des travaux de la plateforme en lien avec le projet.
Le personnel de la plateforme prendra en charge l’ensemble des prestations concernant les virus de transfert de gènes de classe 2 et les immortalisations de lymphocytes en L2. Le laboratoire L3 est en revanche ouvert aux utilisateurs sous réserve de remplir les conditions nécessaires à une activité en L3 et de la validation des projets en amont.
Pour les travaux impliquant des OGM, vous devrez disposer d’une déclaration (OGM de classe 1) ou d’une autorisation (OGM de classe 2 ou 3) de la part de votre laboratoire. Les recherches menées sur des échantillons humains seront déclarées et suivies par un investigateur référent, avec pseudo-anonymisation des échantillons transmis.
Exemple de projet
Des vecteurs viraux de transfert de gènes pour la recherche
La plateforme VVTG est sollicité dans de nombreux projets pour son expertise avancée sur les vecteurs viraux de transfert de gènes. Les vecteurs viraux ont la capacité de transférer du matériel génétique dans les cellules cibles infectées. Ces outils performants et spécifiques sont utilisés pour moduler l’expression de gènes à l’aide de séquences génétiques (shRNA, miRNA) favorisant la surexpression ou répression de ces gènes, mais aussi pour introduire des modifications dans le génome des cellules infectées à l’aide des ciseaux moléculaires CRISPR-Cas9. Les vecteurs viraux de transfert de gènes améliorent la compréhension des mécanismes biologiques, à l’échelle moléculaire et cellulaire. Ils sont d’une aide précieuse pour la recherche de traitements médicaux, en particulier pour la thérapie génique.
Pour en savoir plus : Martin M. et al. (2024). Role of IL-27 in Epstein–Barr virus infection revealed by IL-27RA deficiency. Nature, 628:620-629.
Contact
Plateforme VVTG
SFR Necker, US24 Inserm, UAR3633 CNRS
Faculté de médecine Necker
156-160 rue de Vaugirard
75015 Paris
Région : Île-de-France +33 (0)1 40 61 54 56
+33 (0)1 40 61 54 56
sylvie.fabrega@inserm.fr
Site de la plateforme
THÉMATIQUES : Nouvelles thérapies, vectorisation, cellules souches, organoides
RESPONSABLES SCIENTIFIQUES :
Mathieu Coureuil
RESPONSABLES TECHNIQUES :
Sylvie Fabrega
TUTELLES : AP-HP, CNRS, Inserm, Université Paris Cité
LABELLISATION IBiSA : 2022
MOTS CLÉS : Vectorisation, Nouvelles thérapies, Vecteurs viraux, Transfert de gènes, Production de virus, Dosage de virus, Lentivirus, Rétrovirus, Adénovirus, AAV, AAVr, Infection in vitro et in vivo, Purification par ultracentrifugation, Dosage FACS, Sélection par antibiotiques, Dosage qPCR, Dosage plages de lyses, Immortalisations cellulaires, Lymphocytes B, Lymphocytes T
Fiche mise à jour en 2024










